Generelle forhold
Publisert:
|
Oppdatert:
Endringer
Innhold på siden
Innledning
Terapianbefalingene setter en fellesstandard for forsvarlig og effektiv bruk av antibakterielle midler. En anbefaling har kunnskapsbasert tilnærming der forskning og klinisk erfaring vurderes samlet. Disse anbefalingene er harmonisert med gjeldende regelverk om bruk av legemidler. Veterinærene må til enhver tid følge kravene til forskriving, rekvirering, journalføring og registrering av legemidler i henhold til gjeldende regelverk.
Forordningen om legemidler til dyr ((EU) 2019/6) inneholder flere artikler som omtaler krav og plikter knyttet til veterinærers bruk av legemidler. Terapianbefalingen må derfor leses i lys av forordningens artikler om bruk av legemidler og Mattilsynets veiledning til disse. Veilederen finner du på Mattilsynets nettside.
Valg av antibakterielt middel og administrasjonsvei
-
Hvis det finnes andre fullgode behandlingsmetoder hvor antibakterielle midler ikke benyttes, bør disse velges.
-
Et smalspektret antibakterielt middel som i liten grad påvirker dyrets normalflora bør være førstevalg.
-
3. og 4. generasjons cefalosporiner, polymyxiner til systemisk bruk og kinoloner skal være sistevalg. De skal kun brukes ved akutte livstruende tilstander hvor det antas at behandling med andre antibakterielle midler ikke vil ha ønsket virkning og i de tilfellene hvor dyrkning og resistensbestemmelse viser at andre alternativer ikke kan forventes å ha effekt
-
Langtidsvirkende systemiske antibakterielle preparater skal brukes svært restriktivt fordi det mangler tilstrekkelig dokumentasjon med hensyn til utvikling og spredning av resistens ved bruk av slike preparater.
-
Valg av administrasjonsvei har også betydning for resistensutvikling. I underpunktene her listes administrasjonsvei/type formulering rangert fra laveste til høyeste estimerte påvirkning på utvikling av antibakteriell resistens
-
Lokal individuell behandling (intramammarie, øyedråper, øredråper m.m.)
-
Parenteral individuell behandling (i.v., i.m., s.c.)
-
Oral individuell behandling (tabletter, mikstur m.m.)
-
Oral flokkbehandling via drikkevann/melkeerstatning
-
Oral flokkbehandling via fôr
-
Kategorisering av antibakterielle midler (AMEG kategoriseringen)
Det Europeiske legemiddelbyrået (EMA) har i samarbeid med The Antimicrobial Advice Ad Hoc Expert Group (AMEG) utarbeidet en kategorisering av antibakterielle midler. Kategoriseringen er basert på risikoen de antibakterielle midlene potensielt kan representere for folkehelsen i form av økt antibiotikaresistens når de gis til dyr, balansert mot behovet for substansene til behandling av dyr. Nytte/risikovurderingen bygger på europeisk bruksmønster for antibakterielle midler til dyr og kategoriseringen er derfor ikke fullt ut representative for norske forhold. Kategoriseringen erstatter ikke nasjonale terapianbefalinger og er i første rekke ment som et hjelpemiddel i arbeidet med å utvikle retningslinjer for forsvarlig bruk av antibiotika på nasjonalt nivå.
For ytterligere informasjon se delkapittelet om AMEG – plakaten lenger ned på siden
Farmakologiske betraktninger
Ved valg av antibakterielt legemiddel er det flere forhold som må vurderes:
Følsomhet
-
Bakterien(e) må være følsom(me) for det antibakterielle middelet som velges.
Konsentrasjon på infeksjonsstedet
-
Tilstrekkelig vevskonsentrasjon betinger at legemiddelet absorberes og distribueres til infeksjonsstedet.
-
Antibakterielle midler kan være uladete, svake syrer eller svake baser der ioniseringsgraden, og dermed fettløseligheten, kan påvirkes av pH i vevet. Det er den ikke-ioniserte og fettløselige fraksjonen som krysser biologiske membraner fra blodbanene, ut i vevet og inn i cellene. Forskjeller i pH i ulike vev, f.eks. mellom plasma og melk, har derfor betydning for distribusjon og akkumulering av legemidler og dermed for konsentrasjonen på infeksjonsstedet.
Baktericid/bakteriostatisk effekt
-
Baktericide antibiotika, som for eksempel penicilliner, dreper bakterier. I tilfeller der immunstatusen er nedsatt eller uavklart og allmennpåkjenningen stor bør en som hovedregel velge penicilliner eller eventuelt andre baktericide midler.
-
Bakteriostatiske antibiotika, som for eksempel tetrasykliner, hemmer veksten av bakterier. Immunapparatet eliminerer bakteriene, men dette vil ta noe tid og behandlingstiden er ofte lengre enn for baktericide midler. Noen midler kan være bakteriostatiske ved vanlige terapeutiske konsentrasjoner, men baktericide ved høyere konsentrasjoner.
Tidsavhengig/konsentrasjonsavhengig effekt
-
Effekten av noen antibakterielle midler, for eksempel penicilliner, er tidsavhengig. Dette innebærer at konsentrasjonen av legemiddelet bør ligge over MIC-verdien (Minimum Inhibitory Concentration) for det aktuelle agens i store deler av doseringsintervallet. Å øke konsentrasjonen høyt over MIC for den aktuelle bakterien vil ikke føre til en høyere drapshastighet (gjelder baktericide midler).
-
Andre antibakterielle midler, for eksempel kinoloner og aminoglykosider, har derimot en konsentrasjonsavhengig effekt. Dette betyr at andelen av bakterier som drepes øker med økende konsentrasjon av legemiddelet, men det er ikke så viktig at konsentrasjonen er høy over tid.
Bakteriologi og diagnostikk
Korrekt diagnose er grunnlaget for vellykket behandling. Ved bakterieinfeksjoner er laboratorieundersøkelse en forutsetning for identifisering og resistensundersøkelse av agens. Prøver tas med standardisert teknikk som hindrer forurensing. Prøvene oppbevares kjølig og frostfritt fram til innsending, og kort tid fra prøveuttak til forsendelse bør tilstrebes. Prøvetaking bør gjøres før igangsetting av antibakteriell behandling. Etter påbegynt antibiotikabehandling kan dyrkingsundersøkelser ha begrenset verdi. Prøvetaking etter påbegynt antibakteriell behandling bør likevel gjennomføres dersom innledende behandling ikke har hatt ønsket effekt.
Et negativt bakteriefunn betyr bare at bakterier ikke er funnet i prøvematerialet. Selv om det svekker en mistanke, er det ingen garanti for at den mistenkte bakterien ikke har vært til stede.
Resistensbestemmelse
Testing for resistens kan være av stor verdi for å forutsi eventuell manglende klinisk effekt av antibakterielle midler. Det er av stor betydning at resistensbestemmelsene er standardisert og utføres av laboratorier som benytter kvalitetssikrede metoder. Resistens kan uttrykkes som en MIC-verdi (Minimum Inhibitory Concentration) angitt som mg/l eller som en hemmingssone i mm. MIC-verdien angir den laveste konsentrasjonen av antibiotikumet som er hemmende for bakteriestammen mens hemmingssonen uttrykker antibiotikumets evne til å hemme bakteriens vekst i et vekstmedium. Det er en god korrelasjon mellom en bakteriestammes MIC og diameteren av hemmingssonen.
Ved resistensbestemmelse i laboratoriet klassifiseres bakterier ofte i tre følsomhetskategorier: som sensitive (følsomme), intermediært (moderat) følsomme eller resistente (S-I-R-systemet) overfor ulike antibiotika.
-
En mikrobe er definert som S (følsom) for et antibiotikum når det er stor sannsynlighet for terapeutisk effekt ved standard dosering av antibiotikumet.
-
En mikrobe er definert som I (følsom, økt eksponering) for et antibiotikum når det er stor sannsynlighet for terapeutisk effekt dersom antibiotikumet kan konsentreres på infeksjonsstedet eller ved at man gir en høyere dosering av antibiotikumet enn standard.
-
En mikrobe defineres som R (resistent) mot et antibiotikum når det er liten sjanse for terapeutisk effekt til tross for økt eksponering til antibiotikumet.
Resistensutvikling
Bakterier har ulike mekanismer både for å forandre sitt eget DNA og for å utveksle genetisk materiale seg imellom. Mutasjoner i bakterienes eget DNA oppstår hyppig og nedarves til neste generasjon av bakterier. I tillegg overføres DNA mellom bakterier ved hjelp av genetiske elementer som plasmider, transposoner, integroner og genkassetter. De avgjørende faktorer for resistensutvikling er seleksjon av resistente bakterier som følge av antibiotikabruk og spredning av resistente bakterier. Spredningen av resistente bakterier kan foregå både mellom individer av samme dyreart, mellom ulike dyrearter og mellom dyr og mennesker. Forebygging av sykdom og bekjempelse av antibiotikaresistens tar utgangspunkt i å unngå unødvendig antibiotikabruk og hindre smittespredning.
Det er vist at det er en assosiasjon mellom nivået på forbruket av antibakterielle midler og forekomsten av resistens. Dette gjelder ikke bare målbakterien, men også andre bakterier som er til stede i pasientens normalflora. Resistens-spørsmålet må derfor vurderes i en større sammenheng enn for spesifikke patogener. Miljøbakterier og ikke-patogene kommensaler kan spille en viktig rolle som reservoarer for resistensgener som kan overføres til patogene mikroorganismer.
Ulike antibakterielle midler er forskjellige med hensyn til risiko for resistensutvikling, dynamikk i spredningen og persistens i populasjonen. Smalspektrede antibiotika påvirker relativt få bakteriepopulasjoner mens bredspektrede antibakterielle midler fører til et sterkere seleksjonspress fordi ett større antall bakteriearter påvirkes. Antibakterielle midler som tetrasykliner og fluorokinoloner, som både er bredspektrede og persisterer lenge i miljøet, vil kunne selektere for resistens hos flere bakteriearter () enn smalspektrede midler som også lett brytes ned i miljøet.
Spesielt alvorlige resistensformer
Tiltak for å hindre spredning av alvorlige resistensformer, blant annet ved restriktiv og riktig bruk av antibakterielle midler, er viktig for å opprettholde den gunstige resistenssituasjonen vi har hos dyr i Norge. Spesielt alvorlige resistensformer som meticillinresistente Staphylococcus aureus (MRSA) og multiresistente gram-negative stavbakterier er et økende globalt problem. MRSA er en særlig uønsket resistent mikrobe, siden Staphylococcus aureus er en viktig patogen og meticillin-resistente varianter er motstandsdyktige mot alle betalaktam-antibiotika (penicilliner, cefalosporiner, monobaktamer og karbapenemer). Et viktig mål i det smitteforebyggende arbeidet på humansiden er å hindre introduksjon av MRSA til helseinstitusjoner. Dyre-assosiert MRSA (LA-MRSA) har fått global utbredelse og forekommer særlig hos svin. LA-MRSA har zoonotisk potensiale og smitte til mennesker og andre dyreslag forekommer.
Multiresistente gram-negative stavbakterier, særlig varianter som produserer ekstendert spektrum-betalaktamase (ESBL), er en annen alvorlig resistensform. Denne resistensformen kan bidra til at penicilliner, cefalosporiner og eventuelt også karbapenemer brytes ned. Karbapenemresistens hos Enterobacteriaceae, Pseudomonas spp. og Acinetobacter spp. representerer alvorlige resistensformer som er meldepliktig ved funn hos mennesker i Norge. Genene som ligger til grunn for cefalosporin- og karbapenemresistens er ofte koblet sammen med gener som gir resistens mot andre antibakterielle midler. Dette medfører reduserte terapimuligheter samt økt risiko for ko-seleksjon ved eksponering for antibakterielle midler. Resistensgenene er ofte lokalisert på mobile genetiske elementer som plasmider og/eller transposoner, noe som muliggjør videre spredning av resistensgenene.
Meldeplikt for visse antibiotikaresistente bakterier
Styrket overvåking og oversikt over forekomst av resistente bakterier er viktige tiltak i regjeringens strategi mot antibiotikaresistens. Med endret forskrift om varsel og melding om sykdom, får veterinærer en viktig rolle i dette arbeidet. Fra 1. juni 2019 ble MRSA og flere andre typer antibiotikaresistente bakterier meldepliktige. Veterinærer og laboratorier skal melde fra til Mattilsynet hvis de påviser de de aktuelle antibiotikaresistente bakteriene hos dyr.
For mer informasjon: Når skal du melde fra om resistente bakterier?
Tilgang på antibakterielle midler
Vi får i økende grad legemidler inn på det norske markedet via felleseuropeiske godkjenningsprosedyrer. Dette medfører at det kan komme antibakterielle midler på det norske markedet med en preparatomtale som i liten grad tar hensyn til resistenssituasjonen og behandlingstradisjonene i Norge. Slike antibakterielle preparater kan ha et svært snevert terapeutisk bruksområde under norske forhold og det er viktig at veterinærene legger en kritisk nytte/risikovurdering til grunn ved valg av antibakterielt middel i hvert enkelt tilfelle. Legemidlenes potensiale for å fremkalle resistens, og de potensielle konsekvensene for folke- og dyrehelsen av en situasjon med økt resistens mot den aktuelle substansen, må stå sentralt i denne vurderingen.
AMEG-plakaten
Categorisation of antibiotics for use in animals for prudent and responsible use at EU/EEA level
The Antimicrobial Advice Ad Hoc Expert Group (AMEG) of the European Medicines Agency has recently updated the categorisation of antibiotics based on the potential consequences to public health of increased antimicrobial resistance, when used in animals and the need for their use in veterinary medicine (1). This categorisation does not directly translate into a treatment guideline for use of antibiotics in veterinary medicine but can be used as a tool by those preparing national guidelines.
Veterinarians are encouraged to check the AMEG categorisation before prescribing any antibiotic for animals in their care. The AMEG categorisation does not replace national treatment guidelines, which also need to take account of other factors such as supporting information in the Summary of Product Characteristics for available medicines, constraints around use in food-producing animal species, regional variations in the occurrence of diseases and antibiotic resistance, and national prescribing policies. The brief categorisation (2) as well as the antibiotic classes/sub-classes and substances included in Category A – Avoid and Category B – Restrict (2) is shown below.
AMEG categorisation (2):
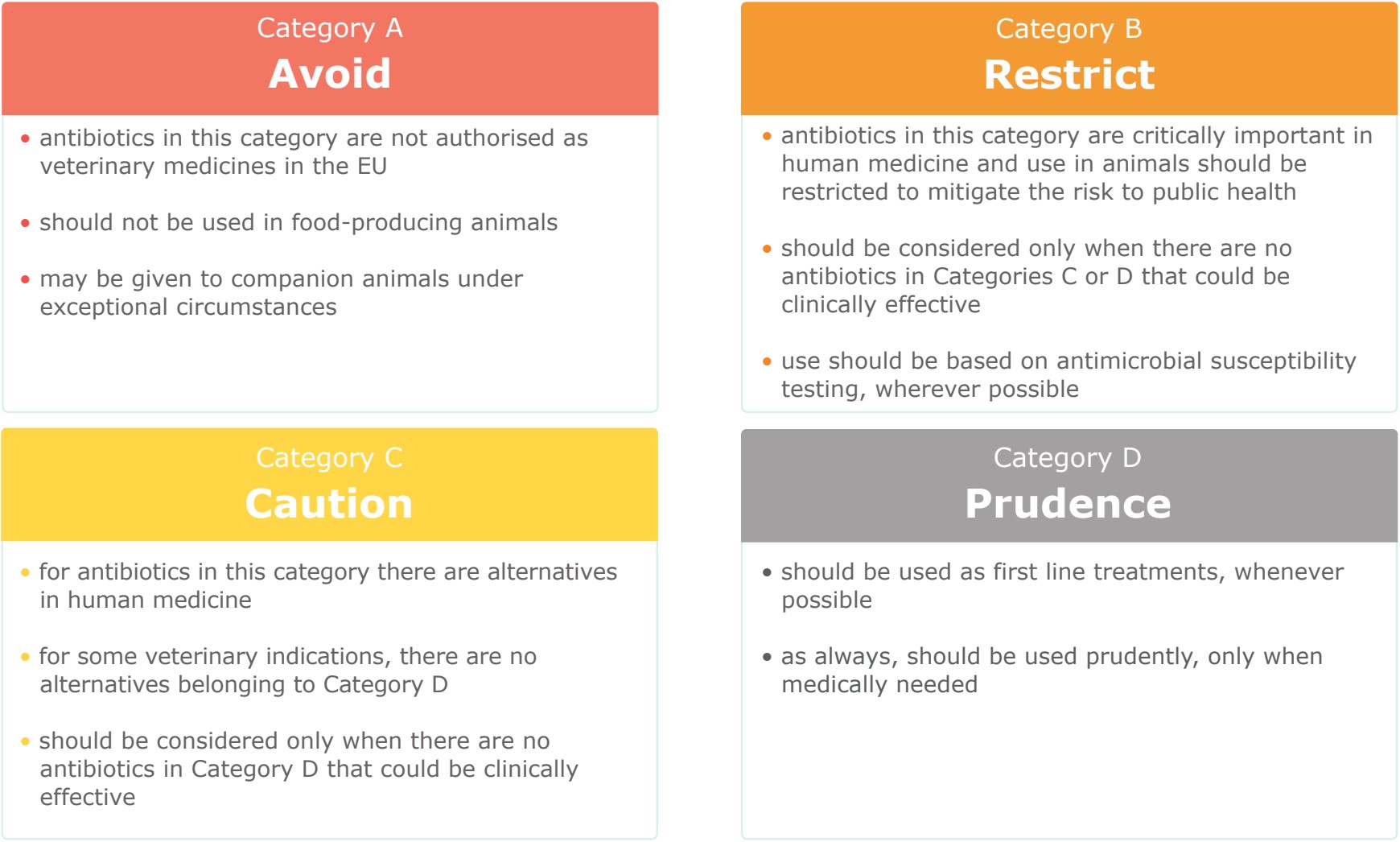
TABLE X. Antibiotic classes/sub-classes and substances included in Category A – Avoid and Category B– Restrict (2).
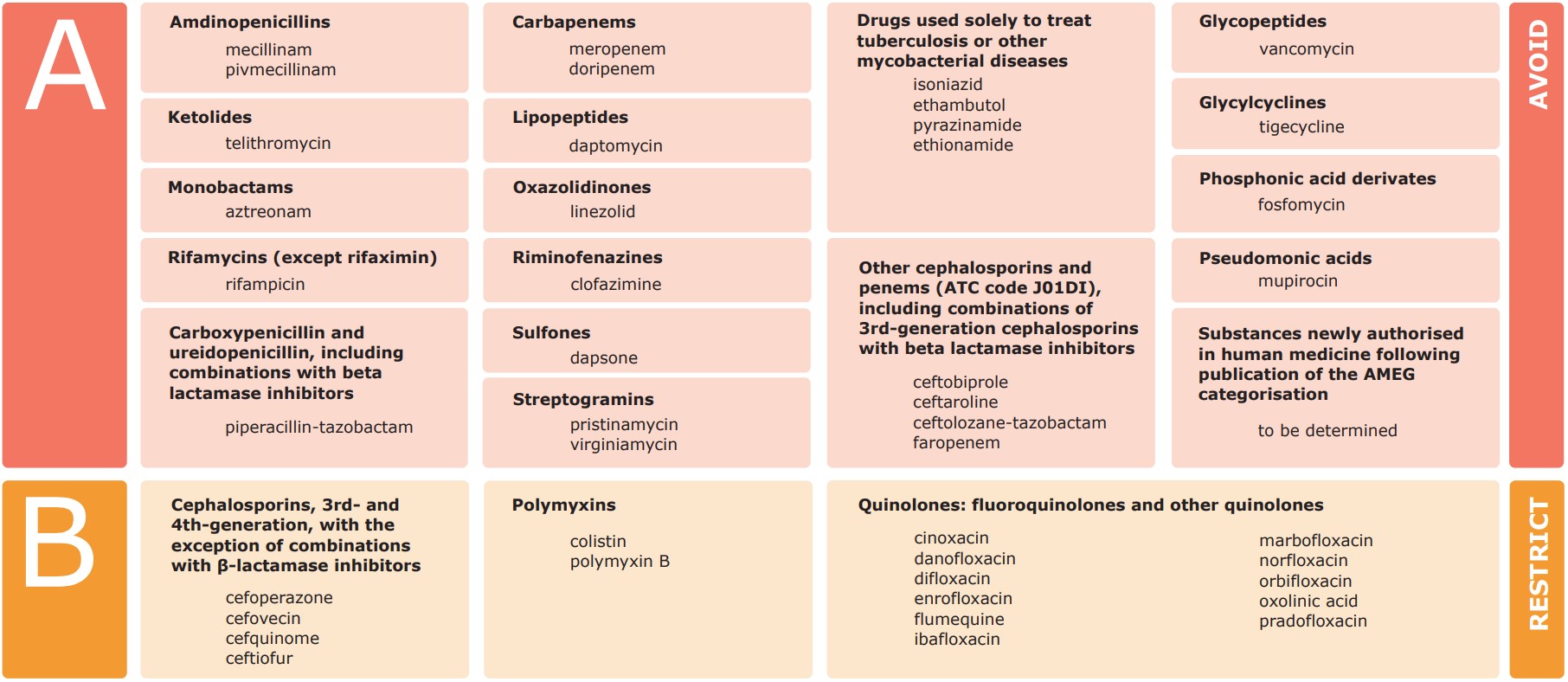
Category B includes the quinolones, 3rd- and 4th-generation cephalosporins and polymyxins. Of note is that these are the same antibiotics as those listed by WHO (3) as the highest priority critical important antimicrobials (HP CIAs) for human medicine; WHO also list macrolides in this category. For the AMEG Category B antibiotics, it is advised that the risk to public health resulting from veterinary use needs to be mitigated by specific restrictions (1).
TABLE Y. Antibiotic classes/sub-classes and substances in Category C – Caution and Category D – Prudence (2).
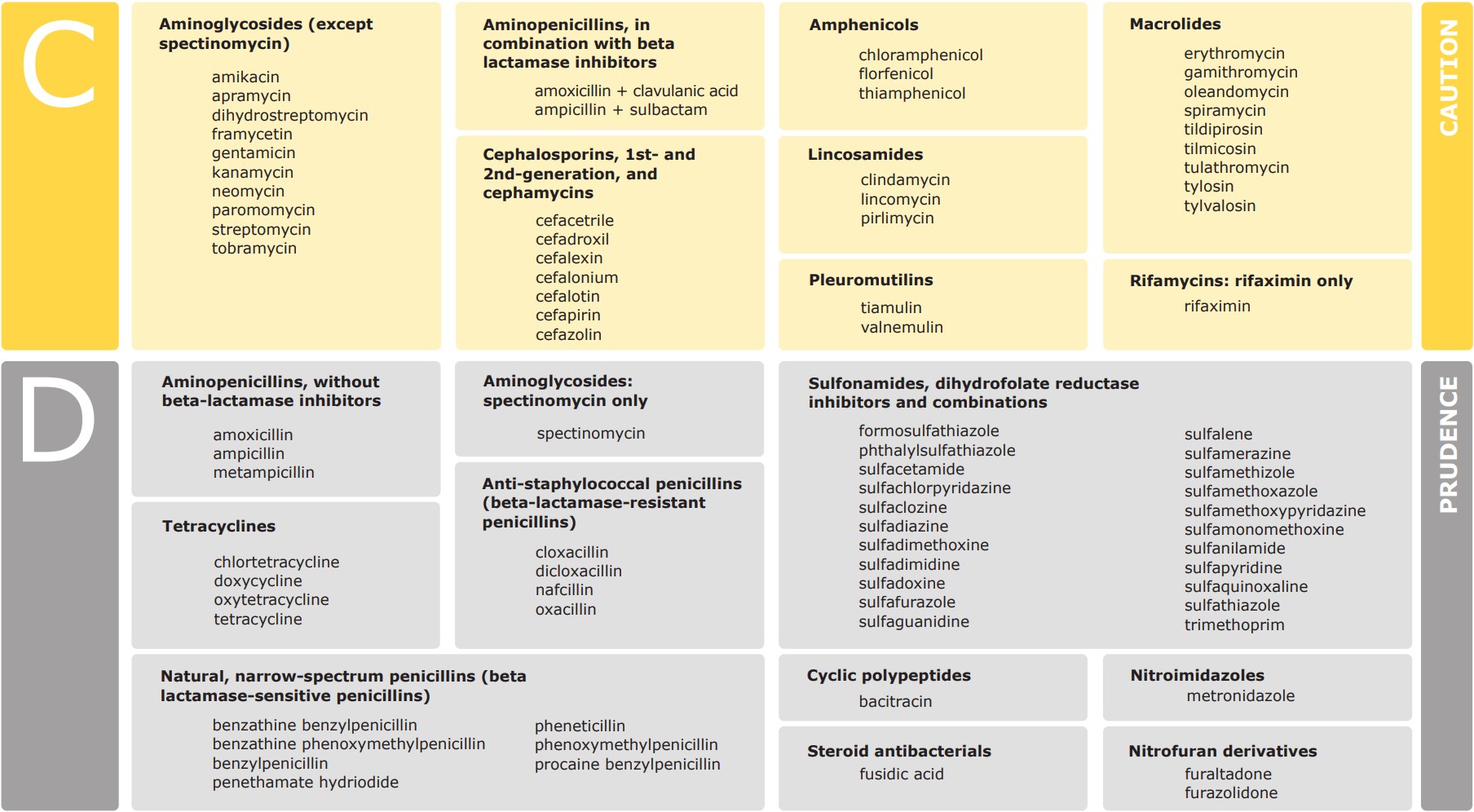
Administration routes
In order to limit exposure of the microbiome, AMEG advices, among others, that the antimicrobial selection pressure should be as local as possible. A suggested listing of routes of administration and formulations, ranked in order from those with in general lower effect on the selection of AMR to those that would be expected to have higher impact on resistance, is shown below (2):

This subsection is based on a simple review of literature (1).
References:
-
EMA/CVMP/CHMP/682198/2017, 2019. Categorisation of antibiotics in the European Union
-
EMA, 2020. Categorisation of antibiotics for use in animals for prudent and responsible use
Categorisation of antibiotics for use in animals (europa.eu)
-
WHO, 2019. 'Critically Important Antimicrobials for Human Medicine (6th revision) 2018 - Ranking of medically important antimicrobials for risk management of antimicrobial resistance due to non-human use',